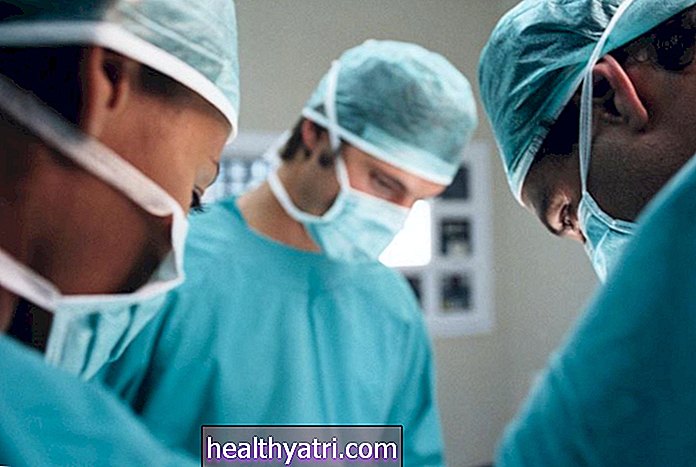
Por lo general, se requiere una biopsia (tomar una muestra del tejido sospechoso para análisis de laboratorio) para hacer el diagnóstico inicial de linfoma. La información del tejido de la biopsia permite a los oncólogos considerar las características moleculares del cáncer, o todos los diferentes matices de los genes y proteínas de las células cancerosas, y aprovechar esa información para optimizar el tratamiento. Por tanto, las biopsias proporcionan a los médicos información vital esencial para el diagnóstico y el tratamiento. A pesar de su indudable valor, las biopsias no están exentas de riesgos y limitaciones.
TEK IMAGE / BIBLIOTECA DE FOTOS DE CIENCIA / Getty Images
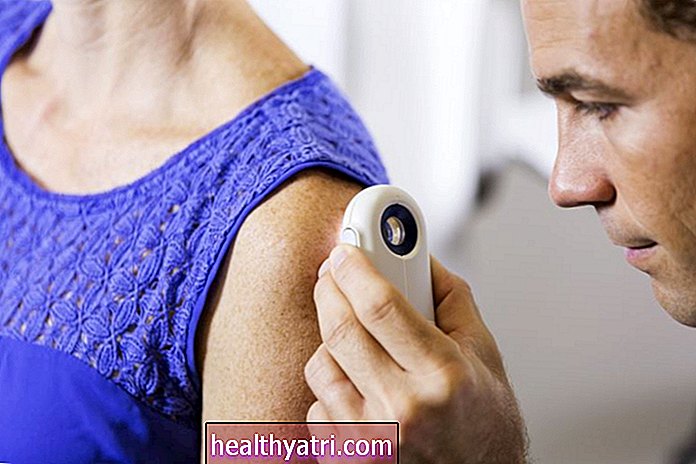
Además, las personas que han sido diagnosticadas con linfomas también necesitan que su enfermedad se "evalúe" en diferentes puntos: inicialmente, para ver qué tan extendida está durante la estadificación; más tarde, para ver que se está reduciendo en respuesta a la terapia; y mucho más tarde, en el seguimiento, para asegurarse de que sus médicos estén al tanto de todo si el cáncer regresa alguna vez después del tratamiento inicial. Una vez más, el valor de las imágenes es innegable, pero las imágenes tienen sus propios inconvenientes, como la exposición a la radiación. Es por eso que estas pruebas se utilizan de forma conservadora para que el beneficio supere los riesgos de exposición.
El futuro: ramificación de biopsias y exploraciones
Hoy en día, el método estándar de oro para evaluar el cáncer como se describe anteriormente son las imágenes. Específicamente, la tomografía computarizada (TC) y la tomografía por emisión de positrones (PET) con fluorodesoxiglucosa (FDG) se utilizan a menudo para la estadificación y para determinar la respuesta del cáncer al tratamiento. A menudo, las dos técnicas se combinan y se denomina PET / CT. Si bien estas pruebas de imagen avanzadas son valiosas y han mejorado la atención al paciente con linfoma, están asociadas con la exposición a la radiación, los costos y, en algunos casos, la falta de precisión.
Todas estas cosas han estimulado el interés de los investigadores en encontrar formas más nuevas, más precisas, menos costosas y menos invasivas de evaluar el cáncer de una persona. Uno de los objetivos es encontrar marcadores específicos, como secuencias de genes, que puedan medirse simplemente mediante un análisis de sangre para controlar el cáncer de modo que, por ejemplo, no tenga que someterse a exploraciones con tanta regularidad durante el seguimiento en el futuro.
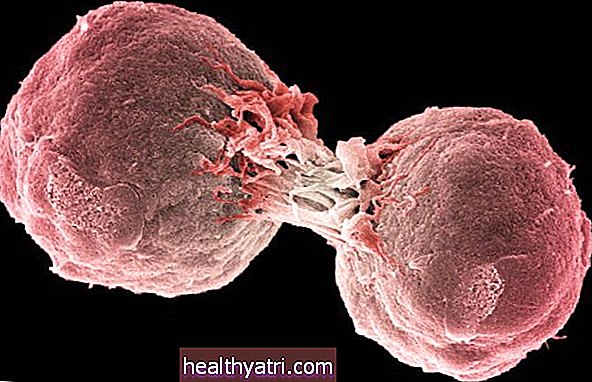
Cuando las células cancerosas mueren, parte de su ADN termina en la sangre. El ADN de las células cancerosas muertas se denomina ADN tumoral circulante o ADNct. Los científicos han desarrollado pruebas para detectar este ADN circulante. Este tipo de enfoque a veces se denomina "biopsia líquida", y los investigadores señalan los posibles beneficios para el seguimiento de la enfermedad, así como para predecir la respuesta de una persona a la terapia desde el principio.
Estudio de ADN de tumores circulantes
En un estudio publicado, los investigadores del Instituto Nacional del Cáncer analizaron la sangre de 126 personas con DLBCL para detectar la presencia de ADN tumoral circulante. El linfoma difuso de células B grandes, o DLBCL, es el tipo más común de linfoma, un cáncer de la sangre que comienza en ciertas células del sistema inmunológico.
A pesar de tener una apariencia similar bajo el microscopio, diferentes subconjuntos de DLBCL pueden tener diferentes pronósticos. Según la Sociedad Estadounidense del Cáncer, en general, aproximadamente tres de cada cuatro personas no tendrán signos de enfermedad después del tratamiento inicial y muchas se curan con terapia.
Sin embargo, el cáncer reaparece en hasta el 40% de las personas y, por lo tanto, a menudo es incurable, especialmente cuando regresa temprano y / o cuando los niveles de células tumorales en la sangre son altos, según el Instituto Nacional del Cáncer.
Todos en la presente investigación habían recibido tratamiento para DLBCL según 3 protocolos diferentes, con fármacos como etopósido, prednisona, vincristina, ciclofosfamida y doxorrubicina, conocida como EPOCH, con o sin rituximab, en ensayos clínicos entre mayo de 1993 y diciembre de 2013.
Se realizaron análisis de sangre antes de cada ciclo de quimioterapia, al final del tratamiento y cada vez que se evaluó la estadificación. Se siguió a las personas durante muchos años después de la terapia y se realizaron tomografías computarizadas al mismo tiempo que los análisis de sangre. Las personas en este estudio fueron seguidas durante una mediana de 11 años después del tratamiento; es decir, el número medio de la serie fue de 11 años, pero las personas fueron seguidas durante períodos más cortos y más largos.
Análisis de sangre predice progresión, recurrencia
De las 107 personas que tuvieron una remisión completa del cáncer, las que desarrollaron ctDNA detectable en las muestras de sangre tenían 200 veces más probabilidades de que la enfermedad progresara que aquellas que no tenían ctDNA detectable.
El análisis de sangre pudo predecir qué personas no responderían a la terapia tan pronto como el segundo ciclo de tratamiento contra el cáncer.
El análisis de sangre también permitió la detección de la recurrencia del cáncer una media de 3,4 meses antes de que hubiera evidencia clínica de la enfermedad, antes de la detección mediante tomografía computarizada.
Actualmente, las biopsias líquidas en DLBCL están en fase de investigación y no están aprobadas ni recomendadas por la FDA por las pautas de la NCCN. La información proporcionada por una biopsia líquida no debe usarse para guiar el tratamiento en el LDCBG.
Direcciones futuras
Todavía hay muchas preguntas sin respuesta y desafíos relacionados con el control de los cánceres utilizando marcadores moleculares de los análisis de sangre, pero la base de conocimientos crece y mejora continuamente.
En el caso del linfoma, y en particular de todos los diferentes tipos de linfoma no Hodgkin, la gran diversidad de estas neoplasias malignas constituye un trabajo desafiante. Incluso cuando se considera la misma malignidad, como DLBCL, es posible que un solo marcador no funcione bien en todos los casos.
Sin embargo, con el tiempo, la esperanza es que algunas de las escisiones, agujas y escáneres tan familiares para los pacientes con cáncer de hoy en día puedan evitarse y reemplazarse por pruebas que detecten estos marcadores y midan sus niveles en el cuerpo.