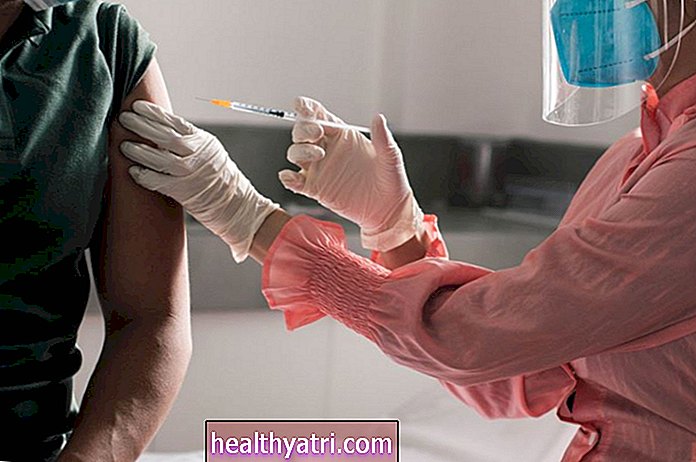
Una advertencia de recuadro negro es la advertencia más severa emitida por la Administración de Drogas y Alimentos de los Estados Unidos (FDA) de que un medicamento puede transportarse y aún permanecer en el mercado en los Estados Unidos.
Aparece una advertencia de recuadro negro en la etiqueta de un medicamento recetado para alertarlo a usted y a su proveedor de atención médica sobre cualquier problema de seguridad importante, como efectos adversos graves o riesgos potencialmente mortales.
UpperCut Images / Getty ImagesUna advertencia de recuadro negro, también conocida como "advertencia de etiqueta negra" o "advertencia de recuadro", se denomina así por el borde negro que rodea el texto de la advertencia que aparece en el prospecto, la etiqueta y otra literatura que describe el medicamento (por ejemplo , publicidad en revistas).
Cuando la FDA requiere uno
La FDA requiere una advertencia de recuadro negro para una de las siguientes situaciones:
- El medicamento puede causar efectos indeseables graves (como una reacción adversa fatal, potencialmente mortal o incapacitante permanente) en comparación con el beneficio potencial del medicamento. Dependiendo de su estado de salud, usted y su médico tendrían que decidir si el beneficio potencial de tomar el medicamento vale el riesgo.
- Una reacción adversa grave puede prevenirse, reducirse en frecuencia o reducirse en gravedad mediante el uso adecuado del fármaco. Por ejemplo, un medicamento puede ser seguro para adultos, pero no para niños. O bien, el medicamento puede ser seguro de usar en mujeres adultas que no están embarazadas.
Informacion requerida
La FDA requiere que el recuadro de advertencia proporcione un resumen conciso de los efectos adversos y los riesgos asociados con la toma del medicamento. Usted y su médico deben conocer esta información cuando decidan comenzar a tomar el medicamento o si deben cambiar a otro medicamento por completo. Comprender los efectos adversos lo ayudará a tomar una decisión mejor informada.
Ejemplos de advertencia
Los siguientes son ejemplos de advertencias de recuadro negro que se han requerido para algunos medicamentos de uso común:
Antibióticos de fluoroquinolonas
Según la FDA, las personas que toman un antibiótico de fluoroquinolona tienen un mayor riesgo de tendinitis y rotura del tendón, una lesión grave que podría causar una discapacidad permanente. La advertencia de la FDA incluye Cipro (ciprofloxacina), Levaquin (levofloxacina), Avelox (moxifloxacina) y otros medicamentos que contienen fluoroquinolona. (Advertencia emitida en julio de 2018.)
Medicamentos antidepresivos
Según la FDA, todos los medicamentos antidepresivos tienen un mayor riesgo de pensamientos y comportamientos suicidas, conocidos como tendencias suicidas, en adultos jóvenes de 18 a 24 durante el tratamiento inicial (generalmente los primeros uno o dos meses). La advertencia de la FDA incluye Zoloft (sertralina), Paxil (paroxetina), Lexapro (escitalopram) y otros medicamentos antidepresivos (advertencia emitida en mayo de 2007).
¿Qué aspecto tiene uno?
El siguiente extracto de la etiqueta de prescripción de Zoloft es un ejemplo de una advertencia de recuadro negro.
El suicidio en niños y adolescentes
Los antidepresivos aumentaron el riesgo de pensamientos y comportamientos suicidas (tendencias suicidas) en estudios a corto plazo en niños y adolescentes con trastorno depresivo mayor (TDM) y otros trastornos psiquiátricos. Cualquiera que esté considerando el uso de Zoloft o cualquier otro antidepresivo en un niño o adolescente debe sopesar este riesgo con la necesidad clínica. Los pacientes que inician la terapia deben ser observados de cerca para detectar empeoramiento clínico, tendencias suicidas o cambios inusuales en el comportamiento. Se debe advertir a las familias y a los cuidadores de la necesidad de una estrecha observación y comunicación con el prescriptor. Zoloft no está aprobado para su uso en pacientes pediátricos, excepto en pacientes con trastorno obsesivo compulsivo (TOC).
Medicamentos opioides
En 2013, la FDA publicó una declaración que detalla el etiquetado de seguridad para toda la clase en todos los analgésicos opioides de liberación prolongada y de acción prolongada (ER / LA). Una parte de estos cambios incluye advertencias en recuadros que indican el riesgo de uso indebido, abuso, dependencia. sobredosis y muerte incluso a las dosis recomendadas.
En 2016, la FDA emitió una guía de etiquetado y advertencias similares para los medicamentos opioides de liberación inmediata.
En conjunto, los cambios son una respuesta directa a la epidemia de opioides que está afectando a los Estados Unidos. Además, la FDA quiere enfatizar que los medicamentos opioides deben usarse solo en los casos de dolor intenso que no se puede tratar de otra manera. En otras palabras, los opioides son drogas peligrosas si no se usan con prudencia y bajo la estrecha supervisión de un médico.
Guías de medicación
Junto con una advertencia de recuadro negro, la FDA también requiere que una compañía farmacéutica cree una guía de medicamentos que contenga información para los consumidores sobre cómo usar de manera segura un medicamento específico. Las guías contienen información aprobada por la FDA que puede ayudarlo a evitar un efecto adverso grave. evento.
Estas guías deben ser entregadas por su farmacéutico en el momento en que surta su receta. Las guías también están disponibles en línea en la compañía farmacéutica y en la FDA. Por ejemplo, la guía de medicamentos para Avandia (rosiglitazona) está disponible en GlaxoSmithKline, el fabricante de Avandia, y en el Centro de Evaluación e Investigación de Medicamentos de la FDA.
Si le preocupa que su medicamento tenga una advertencia de recuadro negro, consulte con su farmacéutico y, si está disponible, obtenga una copia impresa de la guía del medicamento.
Recursos adicionales
El Centro de Información sobre Medicamentos del Centro Médico de la Universidad de Kansas mantiene una lista en línea de todos los medicamentos que tienen una advertencia de recuadro negro. Los medicamentos se enumeran por nombres genéricos. Si está tomando un medicamento de marca, es aconsejable buscar el nombre genérico.










.jpg)